狂犬病疫苗造假,何止“良心去哪儿了”?
近日爆出的狂犬病疫苗造假事件还在持续发酵中。
7月15日,国家药品监督管理局发布通告:国家药监局组织对长春长生生物科技有限责任公司开展飞行检查,发现长春长生在冻干人用狂犬病疫苗生产过程中存在记录造假等严重违反《药品生产质量管理规范》(药品GMP)行为。国家药监局迅速责成吉林省食品药品监督管理局收回长春长生相关《药品GMP证书》,即不允许继续生产狂苗。
16日早上,长生生物发布公告,表示正对有效期内所有批次的冻干人用狂犬病疫苗全部实施召回。
中国网政协频道(《议库》APP平台)小编获悉,目前这次飞行检查所有涉事批次产品尚未出厂和上市销售,全部产品已得到有效控制。
狂犬病疫苗造假事件,让很多人闻之色变。某种程度上来说,把狂犬病疫苗称之为救命药也不为过。长生生物这家知名上市药企为何会出现造假丑闻?疫苗造假事件应当如何杜绝?

此次疫苗造假事件为何广受关注?
其一,是因为狂犬病疫苗的重要性。
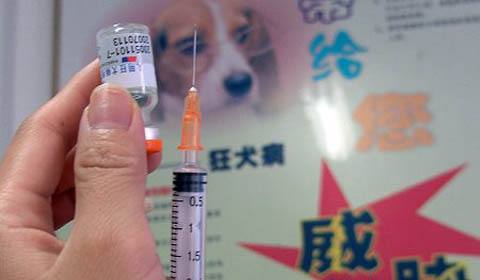
狂犬病疫苗是人被动物咬伤后接种的狂犬疫苗和抗狂犬病血清,预防感染狂犬病。狂犬病是由狂犬病毒所致的自然疫源性或动物源性人畜共患急性传染病,流行性广,病死率极高,对人民生命健康造成严重威胁。
一般来说,投放市场的疫苗是能够达到国家质量标准要求的,但如果疫苗质量欠佳,或没有严格按照规定的条件要求贮藏运输等,会使疫苗质量受到严重影响,导致人为的免疫失败。这就可能直接威胁到疫苗使用者的人身安全,其后果有多严重不言自明。
其二,这次涉事的企业在疫苗市场占有一席之地,而且并非初犯。
据媒体报道,涉事的长春长生公司,并不是什么小企业、小作坊,它已经是国内狂犬疫苗和水痘疫苗的第二大企业,2017年该企业狂犬疫苗签发数量占据国内市场的近四分之一。
据中国产业信息网发布报道称,2017年狂犬疫苗批签发及市场需求情况,目前市场主要生产企业是广州诺诚、辽宁成大、宁波荣安和长生生物,2017年4家企业合计批签发占比88.63%。在狂犬疫苗市场,长生生物2017年的狂犬疫苗销售量占我国市场的23.19%。
长生生物称,从批签数量看,狂犬疫苗和水痘疫苗已经位于国内的第二位。根据长生生物2017年年度报告,公司一类疫苗和二类疫苗的批签发量分别为577万人份和1011万人份,其中公司主要产品冻干人用狂犬疫苗(Vero细胞)、冻干水痘减毒活疫苗、流行性感冒裂解疫苗、冻干甲型肝炎减毒活疫苗的批签发数量分别为355万人份、360万人份、257万人份、272万人份。
2016年、2017年,长生生物的疫苗制品销售量分别达到了1792.9万人份、1784.7万人份。
就在2017年11月3日,这家药企被“点名批评”。当时,原国家食药监总局发布的百白破疫苗效价指标不合格产品处置情况介绍称,在药品抽样检验中检出长春长生生物科技有限公司生产的批号为201605014-01的百白破疫苗效价指标不符合标准规定,并要求长春长生进行整改。
然而这次的“敲打”并没有让这家知名药企“长记性”,还不到一年,长春长生再次被检出问题。
这一次,长春长生的药品GMP生产证书被收回,疫苗生产也全面停止。
这次事件会造成什么影响?
当然,中国网政协频道(《议库》APP平台)小编也提醒各位网友,不必过于恐慌。目前,吉林省食品药品监督管理局已收回长春长生《药品GMP证书》,同时长春长生已按要求停止狂犬疫苗的生产。本次飞行检查所有涉事批次产品尚未出厂和上市销售,全部产品已得到有效控制。为了保证用药安全,长春长生正对有效期内所有批次的冻干人用狂犬病疫苗全部实施召回。根据长春长生近几年对该狂犬病疫苗不良反应的监测,未发现因产品质量问题引起的不良反应。
那么,这次的疫苗问题是如何被发现的?
根据7月15日国家药品监督管理局发布的通告,之所以发现问题是“根据线索,对长春长生开展飞行检查”。有消息称:“本次事件应该是内部举报,国家药监局有因检查,所以暂时仅涉及涉事批次。”
那么,什么是“飞行检查”?飞行检查其实就是突击检查,具有很强的保密性、高效性。尤其是针对举报实施的检查,与以往事先通知被检查企业的跟踪检查相比,飞行检查是一种破除地方保护、揭露并打击行业潜规则、严厉惩戒违法违规行为的强有力手段。
至于通告中提出的“存在记录造假等严重违反《药品生产质量管理规范》行为”,有哪些记录出现造假?目前仍在调查中。中国网政协频道(《议库》APP平台)也将继续关注。
哪些方面可能造假?为何要造假?
北京鼎臣医药资讯创始人史立臣在接受媒体采访时称,企业会出现记录造假的范围较大,“疫苗生产比如说温度上的记录、数量上的记录、人员等涉及生产管理层面的都有可能造假。”,“GMP要求的对关键生产的数据一定要及时准确地记录下来”。
至于出现造假的原因,史立臣表示,一般是为了降低成本,“举个简单的例子,配料应该配100公斤却只用了80公斤,或者应该在某一个温度阶段放24小时,却只放了两个小时”。
另外,长生生物的疫苗一旦停止生产,会对市场造成什么影响?
据悉,虽然长生生物在狂犬疫苗中占有量较高,但长生生物的停止生产,不会造成我国市场上狂犬疫苗缺少的情况。
史立臣也表示,目前国内生产狂犬疫苗的企业较多,“狂犬疫苗的生产数量不取决于企业本身的产能,而取决于相关部门的签发数量。”

疫苗造假问题要如何杜绝?
疫苗问题对公共安全的影响绝不可小视。
根据药品管理法,药品的生产企业未按照规定实施《药品生产质量管理规范》的,给予警告,责令限期改正;逾期不改正的,责令停产、停业整顿,并处五千元以上二万元以下的罚款;情节严重的,吊销《药品生产许可证》。
目前,长生生物疫苗造假事件还未有最终定论,但已经有媒体呼吁,吸取一些国外的经验,将“惩罚性赔偿”的概念引入国内,以解决某些企业作恶成本过低的问题。
所谓的“惩罚性赔偿”,指的是对于有不法行为的企业,除了要赔偿其不法行为造成的损失,还要额外支付一大笔远超其造成损失的“罚金”,以作为警示。最近,著名跨国日化企业强生,就因为售卖可能致癌的爽身粉,而被处以41.4亿美元的巨额惩罚性赔偿,其额度远超5.5亿美元的补偿性赔偿。
有消息称,2017年,长生生物的营收达到15.53亿元,归属于上市公司股东的净利润为5.66亿元。据长生生物财务报告,公司销售疫苗的毛利率达到了86.44%。
在赚钱的同时,长生生物2017年度委托理财发生总金额达到了111.58亿元,但反观长生生物的研发费用,却只有理财总额的1%。2017年,长生生物的研发费用只有营业收入的7.87%。数据显示,2017年长生生物的研发人员数量有153人,研发人员数量占比为14.96%,研发投入金额为1.22亿元。2016年,长生生物的研发投入金额为4333.6万元。
买上百亿理财产品,研发费用却只有区区1.22亿。小编认为,如果对长生生物这类违规违法的企业实行“惩罚性赔偿”,震慑效果或许会提升不少。
事实上,早在2014年,黑龙江省政协委员孙淑红就曾建议,黑龙江省应实行市场准入制,加大对疫苗等相关保健食品、药品的监管检验力度。
2014年,全国政协委员朱成钢也曾提交过提案——《疫苗接种不良反应受害者的救助和补偿机制亟待完善》,关注接种疫苗后产生不良反应的受害者群体。朱成钢认为,疫苗案最为挑动大众的神经。如果我们对于异常反应的救助补偿机制足够完善,大家或许会更理性地对待。
疫苗问题向来都牵动着大众神经。中国网政协频道(《议库》APP平台)也将持续关注这次事件的进展。
资料来源:央视网、中国青年报、北京日报、新京报、中国产业信息网、人民政协网、生活报等
转载请标明:中国网政协频道(《议库》APP平台)
推荐阅读:




